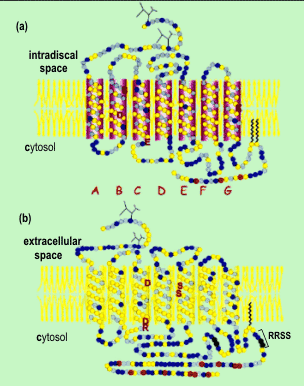
Na+,К+-АТФаза (ATPаза) (a): взаимодействия доменов при рецепции кардиогликозида
Современная модель рецептора сердечных гликозидов К+-АТФазы предусматривает определенную геометрию различных локусов рецептора и индукцию конформационных изменений в них при связывании ингибитора (кардиогликозида).
Известно, что сердечные гликозиды - специфические ингибиторы Nа+,К+-АТФазы, стабилизируя фермент в функционально неактивной конформации, подавляют все типы энзиматических и транспортных процессов, осуществляемых Na+,К+-АТФазой [ Болдырев ea 1985 , Кравцов ea 1990 ], и, следовательно, препятствуют конформационным перестройкам, обусловленным энзиматическими реакциями [ Robinson ea 1993 ].
В то же время кажущееся сродство Nа+,К+-АТФазы к уабаину тесно связано с ферментативным циклом [ Болдырев ea 1985 , Кравцов ea 1990 ]. Таким образом, рецепция уабаина является маркером конформационных состояний Ка+,К+-АТФазы [ Robinson ea 1993 ].
Показано, что уабаин с наибольшей скоростью связывается с Е2-Р-формой фермента [ Болдырев ea 1985 , AnnerB.M. ea 1985 ], а конформационный переход Е1- Е2 сопряжен со структурными изменениями, затрагивающими и внутримембранные сегменты. В частности, в конформации Е1, по сравнению с Е2 наблюдается снижение включения в a-субъединицу маркеров аминокислот, контактирующих с липидами, что свидетельствует о структурной реорганизации внутримембранных доменов при ферментативном цикле [ Modyanov ea 1992 ]. Это предполагает наличие также и конформационных изменений рецепторной части Nа+,К+-АТФазы, благоприятных для связывания гликозидов.
С другой стороны, установлено, что в присутствии уабаина меняется картина химотриптического гидролиза а-субъединицы и происходит дополнительное расщепление ее фрагмента с мол. массой 78 кДа на фрагменты 40 и 35 кДа [ Castro ea 1979 ]. Следовательно, уабаин индуцирует изменение пространственной структуры молекулы Na+,К+-АТФазы [ Модянов ea 1988 ], в частности конформации ее цитоплазматических доменов [ Kirley ea 1991 ]. Последнее утверждение основано на результатах исследований, согласно которым связывание уабагенина индуцировало снижение способности остатков Цис-367 и Цис-656, локализованных на цитоплазматических доменах фермента вблизи центра фосфорилирования и АТФ-связывающего участка соответственно, вступать в реакцию с N-(1-пирен)малеимидом [ Kirley ea 1991 ]. В свою очередь, N-(1-пирен)малеимид также ингибирует связывание уабаина в результате аллостерического эффекта, через изменение степени фосфорилирования фермента. Не исключено, что уабаин стабилизирует фермент в особой конформации [ Robinson ea 1993 ].
Кроме того, Аннер и соавт. [ Anner ea 1989 ] высказали предположение о существовании взаимосвязи между резистентностью рецепции и особенностями в транспорте ионов натрия Na+,К+-АТФазой почек крысы, сопровождающейся, очевидно, модификацией Ка+-связывающего участка по сравнению с гликозидчувствительной формой из почек кролика.
Также установлена способность уабаина наряду с Rb+ защищать С-концевую часть а-субъединицы Nа+,К+-АТФазы при исчерпывающем трипсинолизе [ Lutsenko ea 1994 ]. Поскольку домены, окклюдирующие одновалентные катионы, образованы внутримембранными сегментами [ Robinson ea 1993 , Shainskaya ea 1994 ], а после протеолиза уабаин остается прочно связанным с мембраной и сохраняется антагонизм уабаина и Rb+, предполагается, что связывание уабаина "замораживает" внутримембранную часть а-субъединицы в стабильном, подобном окклюдированному состоянии [ Lutsenko ea 1994 ].
Следовательно, в основе ингибирующего действия уабаина лежит реорганизация внутримембранной части белка в ответ на связывание ингибитора с внеклеточными доменами, а не изменение конформации внутриклеточных доменов [ Lutsenko ea 1994 ].
Показано, что при замене акцептора фосфата Асп-369 - Асн в активном центре а1-изоформы Na+,K+-АТФазы овцы, сопровождающейся подавлением АТФазной активности, не утрачивается способность фермента к связыванию уабаина с высоким сродством в присутствии Mg2+, хотя и подавляется способность АТФ и Фн стимулировать этот процесс [ Kuntzweiler ea 1995 ]. Следовательно, образование b-аспартил-фосфорилированного интермедиата не требуется для связывания ингибитора. У мутантного фермента катионсвязывающие свойства не меняются и сохраняется антагонизм одновалентных ионов и уабаина, что свидетельствует о взаимосвязи иониндуцированных конформационных изменений внутримембранных доменов и рецепторной части молекулы Na+,К+-АТФазы.