Аллогенная ингибиция: заключительный обзор
При изучении процессов ткане- и видоспецифической клеточной адгезии исследователи, пытаясь понять действующие силы этих клеточных отношений, предполагают наличие определенных неидентичных белков мембраны, которые, являясь взимно комплементарными, осуществляют физическую связь между клетками. Иначе, они выдвигают принцип "+/- комплементарности" или "лиганд-рецепторного взаимодействия", действующий при ткане- и видоспецифическом клеточном кооперировании.
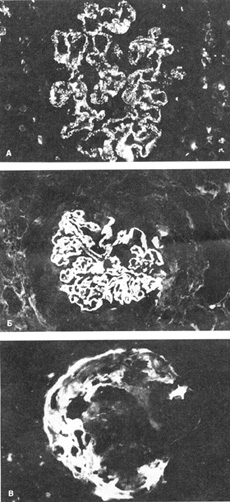
Существует и другая точка зрения, предполагающая взаимодействие по принципу "своего" со "своим". Возможный механизм снижения колониобразующей способности клеток костного мозга в генетически отличающемся организме и фенотипическая коррекция возникающего подавления представлены на рис. 11.11 . Прекурсорные кроветворные клетки, введенные в сингенный организм, образуют определенное число колоний. Начало роста колоний зависит от эффективности взаимодействия прекурсора со стромальными элементами селезенки , на которой и формируются КОЕ . Среди компонентов мембранных клеточных структур, обеспечивающих полноценное взаимодействие, представлены и антигены гистосовместимости . При нарушении сингенности клеточного взаимодействия (введение клеток костного мозга родителей в гибрид) подавляется процесс нормального клеточного взаимодействия. Это явление получило название аллогенной ингибиции (гибридной резистентности) . Инкубация клеток костного мозга одного из родителей с пре-мРНК второго родителя или гибрида F1 определяет экспрессию на поверхности культивируемых клеток антигенов донора РНК. Этот процесс собственно и обеспечивает восстановление сингенных отношений между донором и стромальными элементами хозяина, вследствие чего наблюдается восстановление колониеобразования.
Одно из возможных объяснений этой феноменологии как раз и состоит в представлении о способности антигенов гистосовместимости вступать между собой в контакт, действующего по принципу взаимодействия "своего" со "своим".
Описанные в этом разделе факты являются основой для формирования направления исследований, задачей которого является экспериментальное и теоретическое решение проблемы фенотипической коррекции клеток как специфически управляемого процесса. Иначе это направление можно было бы назвать клеточной инженерией.
В 1961 году М.Бернет выдвинул и обосновал положение, согласно которому роль иммунитета сводится не только к обеспечению антиинфекционной защиты, но и к поддержанию генетической целостности соматических клеток, составляющих организм. Явление аллогенной ингибиции представляет другой дополнительный механизм, имеющий то же предназначение, что и иммунитет. Действительно, данные экспериментов демонстрируют, что даже незначительные генетические различия между донором клеток и реципиентом, в частности по минорным антигенам гистосовместимости, приводят к аллогенному подавлению жизнеспособности таких клеток. Из этого следует, что мутационные изменения клеток тела, определяющие антигеннную клеточную модификацию, могут привести к подавлению жизнеспособности мутантных клеток в организме, ставшем для них генетически чужеродным.
Таким образом, аллогенная ингибиция, как и специфический иммунитет, выступает в качестве фактора стабильности онтогенеза и тем самым обеспечивает передачу наследственного материала от поколения к поколению.