Src-киназы: регуляция: механизм
SH2- и SНЗ-домены играют ключевую роль в регуляции каталитической активности киназ семейства Src.
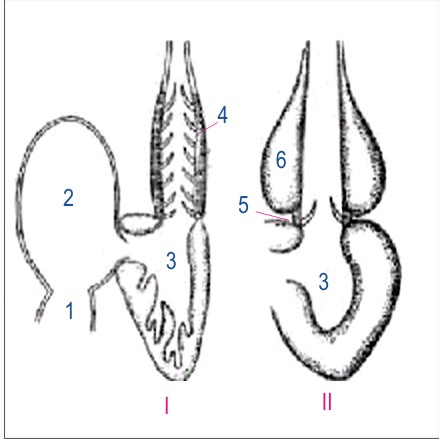
Результаты рентгеноструктурного анализа позволили объяснить, как внутримолекулярные взаимодействия SH2 и SH3 стабилизируют неактивную конформационную структуру этих киназ. Оба этих домена прилегают к киназному домену с противоположной к каталитической щели стороны. SH3-домен взаимодействует с последовательностями в каталитическом домене и с последовательностями линкерной зоны, лежащей между SH2 и каталитическим доменами ( рис. 2 ) [ Xu W. et al, 1999 ].
SH2-домен взаимодействует с фосфотирозином 527, локализованным в С-терминальной области белка. Туr-527 в c-Src и соответствующие тирозины в других РТК являются участками первичного фосфорилирования in vivo. Это основание фосфорилируется цитоплазматической киназой Csk [ Nada S. et al, 1991 ].
Утрата Туr-527 или его дефосфорилирование приводят к стимуляции каталитической активности Src.
Этот вывод сделан на основании ряда экспериментальных данных: замена Туr-527 на другую аминокислоту конститутивно активизирует c-Src [ Kmiecik Т.Е. and Shalloway D., 1987 ]; данный участок отсутствует в белке v-Src [ Reynolds A.B. et al, 1987 ]; нарушение активности гена csk влечет за собой увеличение активности РТК семейства Src [ Imamoto J. and Soriano P., 1993 ].
Таким образом, предполагается, что фосфорилирование С- концевого тирозина под действием киназы Csk обусловливает внутримолекулярное взаимодействие этой области с SH2-доменом, что сохраняет белок Src в закрытой инактивированной форме.