T-Бокс регуляция у грамположительных бактерий
В начале этого обзора мы рассмотрели регуляцию экспрессии аминокислотных оперонов E. coli при помощи лидерного пептида, скорость трансляции которого зависела от доступности определенной аминоацилированной тРНК в клетке, а также регуляцию экспрессии у B. subtilis при помощи специального стимулирующего терминацию белка, который активируется избытком аминокислоты. У грамположительных бактерий экспрессия генов, продукты которых необходимы для биосинтеза белка, также усиливается в условиях дефицита соответствующей аминокислоты, однако сигналом дефицита зачастую служит не отсутствие аминокислоты или аминоацилированной (заряженной) тРНК , а наоборот, избыток неаминоацилированной (незаряженной) тРНК. Построенный на избытке незаряженной тРНК механизм регуляции называется T-бокс регуляцией. Общая схема такой регуляции показана на Рис. 5 .
Как и в других аттенюаторных системах, лидерный транскрипт здесь может образовывать альтернативные структуры, терминатор или антитерминатор. В генах, которые регулируются по механизму T-бокс зависимой аттенюации транскрипции , насцентный транскрипт может формировать две альтернативных структуры, стабильный внутренний терминатор транскрипции или же менее стабильную антитерминаторную структуру. Незаряженная тРНК способна узнавать участок РНК, и при связывании значительно стабилизировать антитерминаторную структуру, приводя к полноразмерной транскрипции соответствующего оперона; при достаточном уровне заряженной тРНК транскрипция преждевременно терминирует и экспрессии структурных генов оперона не происходит. Таким образом, благодаря T-бокс регуляции энергозатратный de novo биосинтез аминокислот запускается только при их недостатке в окружающей среде. Важную роль в связывании играет специальный участок-спецификатор (specifier sequence), который повторяет кодон соответствующей аминокислоты и узнается антикодоновой петлей тРНК . В некоторых случаях в составе шпильки находится сайт связывания рибосомы, последовательность Шайна-Дальгарно , которая высвобождается при связывании тРНК, и таким образом регуляция происходит не на транскрипционном, а на трансляционном уровне [ Green, 2010 ].
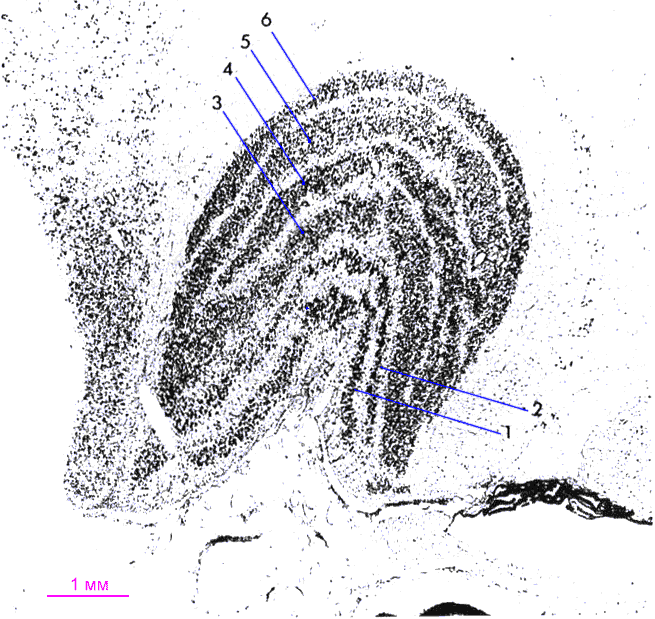
Механизм T-бокса был открыт благодаря тщательному сравнительному анализу нескольких оперонов, кодирующих аминоацил-тРНК-синтетазы B. subtilis [ Grundy, 1993 ; Henkin, 1992 ]. Все эти опероны содержали лидерные последовательности длиной около 300 нт, гипотетические вторичные структуры которых показаны на Рис. 6 . При сравнении выяснилось, что все структуры весьма схожи и включают терминатор транскрипции, короткую консервативную последовательность, названную T-боксом, и несколько шпилек. Последовательности, образующие ножки шпилек, довольно сильно различались, тогда как последовательность РНК в выпетливаниях оказалась очень консервативна. Исследователи заметили, что в определенном участке выпетливания одной из шпилек содержится кодон той аминокислоты, за синтез которой отвечает оперон. Эту последовательность назвали спецификатором. Единичная замена в спецификаторе UAC (Tyr) в лидерном участке tyrS (кодирует тирозиновую аминоацил-тРНК-синтетазу) на UUC (Phe) приводила к индукции тирозинового оперона недостатком фенилаланина, а не тирозина, а введение в этом участке нонсенс-кодона приводило к получению неиндуцибельного штамма. Введение нонсенс мутации в супрессирующий штамм, тРНК(Lys) которого узнает нонсенс-кодон, приводило, в свою очередь, к индукции экспрессии tyrS оперона при недостатке лизина. Единичные замены в других уча-стках лидера не приводили к таким радикальным эффектам, наводя на мысль, что для регуляции имеет решающее значение именно связывание антикодона тРНК с соответствующим кодоном [ Grundy, 1993 ]. Позднее такое взаимодействие было показано напрямую для оперона glyQS с использованием синтезированной in vitro синтезированной тРНК(Gly) [ Grundy, 2002 ] и оперона thrS с использованием очищенной тРНК(Thr) B. subtilis [ Putzer, 2002 ]. В таких системах добавление соответствующей тРНК in vitro стимулировало антитерминацию в отсутствие дополнительных белковых факторов. Антитерминация происходила также в гетерологичной системе с использованием РНКП E. coli [ Grundy, 2002 ].
Детальная структура лидерной последовательности tyrS оперона B. subtilis представлена на Рис. 7 . Базовый лидер в T-бокс системе содержит три шпилечных домена (шпильки I, II и III), псевдоузел (шпилька IIA/B), предваряющий T-бокс, и терминатор транскрипции. Собственно T- боксом называется консервативная последовательность длиной 14 нт, отвечающая за переключение между двумя альтернативными структурами.
Стоит отметить, что в описанных выше опытах добавление фенилаланина к клеткам, содержащим замену тирозинового кодона спецификатора на фенилаланиновый, приводило к индукции экспрессии оперона tyrS более слабой, чем при добавлении тирозина к клеткам дикого типа, что говорит о существовании дополнительных детерминант специфичности помимо последовательности специ-фикатора.
Биоинформатический поиск и анализ позволил выявить более тысячи T- бокс систем. Сравнение различных систем показало, что, как и в некоторых случаях аттенюации транскрипции посредством трансляции лидерного пептида [ Elf, 2003 ], в составе спецификатора преимущественно используются редкие кодоны [ Vitreschak, 2008 ], вероятно, для повышения чувствительности системы к концентрации соответствующей аминокислоты [ Elf, 2003 ].
Две трети (62%) найденных T-бокс регуляторов находятся перед оперонами тРНК-синтетаз, но также есть опероны биосинтеза (18%) и транспорта (12%) аминокислот, и гены неизвестной функции [ Green, 2010 ]. По всей видимости, первичным объектом регуляции T-бокс системами были именно гены аминоацил-тРНК синтетаз в группе Firmicutes , а позднее, вследствие внутригеномных дупликаций и горизонтального переноса генов, эти регуляторные блоки распространилась на другие опероны и даже другие группы организмов [ Vitreschak, 2008 ]. Так, хотя T-боксы в целом нехарактерны для грамотрицательных организмов , были найдены лейциновые T-боксы в оперонах биосинтеза лейцина у дельтапротеобактерий [ Vitreschak, 2008 ]. Важно отметить, что для T-бокс регуляции не требуется никаких дополнительных белковых факторов, необходимы и достаточны тРНК-РНКовые взаимодействия. По механизму действия T-бокс системы весьма близки к рибопереключателям - еще одному пути осуществления аттенюации транскрипции.