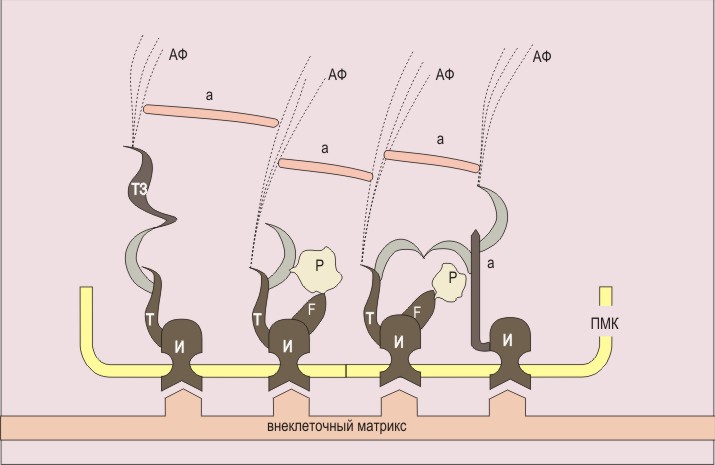
RAS-зависимая регуляция аденилатциклазы
Ген cdc35 ( cyr1 ), кодирующий аденилатциклазу , был проклонирован многими исследовательскими группами ( Matsumoto et al., 1982 ; Boutelet et al., 1985 ; Casperson et al., 1985 ; Kataoka et al., 1985a ; Powers et al., 1984 ). Удалось маркировать многие гены, взаимодействующие с аденилатциклазой.
По гомологии с онкогенами ras млекопитающих проклонированы гены RAS1 и RAS2 ( DeFeo-Jones et al., 1983 ). Продукты этих генов (RASp) относятся к G-белкам (ГТФ-связывающим белкам) ( De Vendittes et al., 1986 ; Temeles et al., 1985 ; Tamanoi et al., 1984 ). Эти белки передают сигнал от рецептора. Они состоят из субъединиц альфа, бета, гамма. При активации альфа-субъединица G-белка связывает ГТФ и отсоединяется от субъединиц бета и гамма. При гидролизе ГТФ до ГДФ G-белок инактивируется.
Белки RASp дрожжей обладают большим молекулярным весом, чем аналогичные белки высших эукариот. При этом два из трех доменов RASp консервативны, и длина их одинакова у всех исследованных RASp. Различия между белками дрожжей и высших эукариот набдюдаются в третьем С-концевом неконсервативном домене, размеры которого у сахаромицетов много больше, чем у высших эукариот. Этот домен необходим для локализации RAS1p и RAS2p на плазматической мембране ( Fujiyama, Tamanoi, 1986 ).
Гены RAS1 и RAS2 контролируют жизненно важные функции - их oдновременная дизрупция приводит к летальности. RAS2 компенсирует мутацию ras1: дизрупция RAS1 не сказывается на фенотипе. Дизрупция RAS2 приводит к накоплению гликогена и трегалозы, индукции споруляции на полной среде у MATa/MATalfa и неспособности расти на ацетате и этаноле ( Breviario et al., 1986 ; Tatchell et al., 1985 ; Fraenkel, 1985 ; Kataoka et al., 1984 ). При гиперэкспрессии на плазмиде ген RAS1 полностью компенсирует дизрупцию гена RAS2. Разница в эффектах дизрупции связана с различиями в контроле транскрипции и трансляции. Транскрипция и трансляция RAS1 подавляются в стационаре и на неферментируемых источниках углерода ( Breviario et al., 1986 ).
Двойные мутанты ras1ras2 (и мутанты RAS1ras2 на этаноле) проявляют фенотип, сходный с cyr1 ( cdc35 ) . Добавление очищенного белка RAS восстанавливает аденилатциклазную активность ( Toda et al., 1985 ). Продукт RAS2 стимулирует очищенную аденилатциклазу in vitro ( Fields et al., 1988 ).
RAS-белки сахаромицетов и млекопитающих функционально взаимозаменимы. RAS1 дрожжей может вызвать злокачественную трансформацию клеточной структуры млекопитающих ( DeFeo-Jones et al., 1985 ). На-ras млекопитающих компенсирует летальность, вызываемую дизрупцией ras1 и ras2 ( Kataoka et al., 1985b ). Вместе с тем у млекопитающих белки RAS не взаимодействуют с аденилатциклазой и не влияют на концентраци внутриклеточной цАМФ - в этом их отличие от RASp сахаромицет.
In vitro сконструирована мутация, приводящая к замене в положении 19 аминокислотной последовательности белка RAS2p лейцина на валин ( RAS2val19 ). В этом случае белок RAS не способен гидролизовать ГТФ и находится в постоянно активированном состоянии. У млекопитающих подобные мутации приводят к превращению протоонкогена в онкоген . У дрожжей мутация RAS2val19 доминантна и приводит к неспособности останавливать митотический цикл при голодании по глюкозе и азоту, а также при термошоке (т.e. к неспособности развивать стрессовую реакцию ) ( Toda et al., 1985 ). Очевидно, при этом наблюдается конститутивная активация аденилатциклазы.
Найдены модуляторы функции белков RAS. Один из них - это ген cdc25 , мутации в котором приводят к тому же прототипному фенотипу, что и cdc35. Этот ген был проклонирован несколькими группами исследователей ( Robinson et al., 1987 ; Brock et al., 1987 ; Martegani et al., 1986 ; Camonis et al., 1986 ; Toda et al., 1985 ). При рестриктивной температуре у мутантов снижен уровень цАМФ ( Camonis et al., 1986 ). Мутация RAS2val19 супрессирует мутацию cdc25 ( Baroni et al., 1989 ).
У мутантов RAS2val19 были отобраны ревертанты, которые (как и у штаммов дикого типа) характеризовались устойчивостью к термошоку (т.е. останавливали митотический цикл в этих условиях). Оказалось, что реверсия произошла за счет второй мутации в гене RAS2 в области, кодирующей домен связывания с фосфатной группой молекулы ГТФ. У одного из реверантов ( RAS2val19gly22 ) эта мутация привела к замене в 22 положении аминокислотной последовательности глутамина на глицин, а у второго реверанта ( RAS2val19Ala25 ) к замене глутамина на аланин в 25 положении. Устойчивость к термошоку у этих реверантов проявлялась в компаунде с аллелью RAS2val19 , но не в гетерозиготе с RAS2+ . При сверхэкспрессии CDC25, введенного в клетки в составе многокопийной плазмиды, устойчивость к термошоку проявлялась и в компаунде с аллелью дикого типа RAS2+. Эти данные указывают на взаимодействие продуктов генов RAS2 (RAS2p) и CDC25 (CDC25p). Предположили, что белок CDC25p , связываясь с RAS2p, способствует отщеплению от него ГДФ (образовавшейся вследствие гидролиза ГТФ), после чего возможно связывание белка RAS2p с новой молекулой ГТФ, приводящее к активизации этого белка. У мутанта cdc25 белок RAS2p постоянно находится в неактивном состоянии. Мутация RAS2val19 эписталирует мутацию cdc25, так как белок RAS2val19р постоянно связан с молекулой ГТФ. У реверантов RAS2val19Ala25 и RAS2val19gly22 восстанавливается способность белка RAS2p гидролизовать ГТФ ( Powers et al., 1989 ). Во взаимодействии с белком CDC25 участвует вариабельный С-терминальный домен RASp ( Marchall et al., 1987 ).
Выделен ген SCD25 , который также, как и CDC25 регулирует диссоциацию комплекса RASp-ГДФ. С-концевые домены продуктов этих генов, взаимодействующие с RASp, сходны. Дизрупция SCD25 не приводит к летальности, то есть в отличие от CDC25, SCD25 не является жизненно важным ( Damak et al., 1990 ).
Клонировали еще два модулятора функции генов RAS: ген IRA1 и ген IRA2 . Дизрупция гена IRA1 повышает чувствительность клеток дрожжей к термошоку и голоданию. У гомозигот ira1/ira1 невозможна индукция споруляции . При изучении генных взаимодействий оказалось, что мутация ira1 супрессирует летальный эффект мутации cdc25, но не способна супрессировать летальный эффект мутации cdc35, а также летальный эффект, обусловленные мутациями в генах RAS1 и RAS2. Двойные мутанты ira1cdc25 не только жизнеспособны, но и устойчивы к термошоку, т.е. проявляют дикий фенотип. У мутантов ira1 и ira2 повышен уровень внутриклеточного цАМФ, накапливаются RASp в ГТФ-связывающей форме. Полагают ,что IRA1p и IRA2P - антагонисты CDC25p, которые стимулируют переход RASp из ГТФ-связывающей формы в ГДФ-связывающую. Эту гипотезу подтверждает наличие в IRA1p и IRA2p домена, гомологичного одному из участков белка млекопитающих GAP, активирующего ГТФ-азную активность G-белков ( Tanaka et al., 1990 ; Tanaka et al., 1989 ).
Еще один ингибитор функции RAS - продукт гена MSI1 ( Ruggieri et al., 1989 ). Сверхэкспрессия этого гена супрессирует мутации RAS2val19 и ira1.