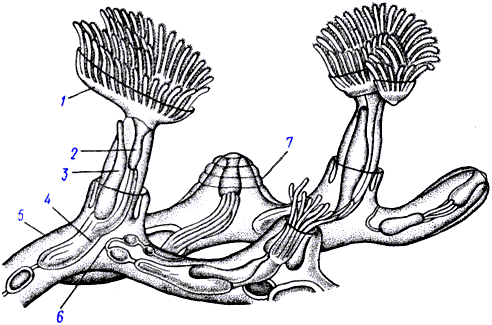
IP3R (IP3-рецептор): структура
Рецепторы инозитол-1,4,5-трисфосфата проявляют заметное сходство в организации с RyR . Как уже отмечалось, все члены этих двух семейств являются тетрамерами, состоящими из больших субъединиц с молекулярной массой 310 и 560 кД, соответственно. Значительная степень гомологии между двумя семействами обнаруживается в домене, локализованном в COOH- конце, который шестикратно пронизывает мембрану и участвует в образовании канала. Оба типа каналов имеют геометрическую форму цветной капусты- (вид в профиль) или розетки (вид спереди), приблизительно одинаковой ширины порядка 20 нм, но разной высоты: 10 и 18 нм для IP3 и рианодинового рецептора, соответственно. Белок состоит из восьми трансмембранных доменов, формирующих проводящий канал для катионов. Вся остальная часть молекулы располагается на цитоплазматической стороне, где имеются места связывания IP3 , Са2+ , ATP , а также два остатка Ser, фосфорилируемых PKA и PKG .
Было показано, что PKC и CaKMPK также фосфорилируют IP3R, встроенный в липидные везикулы. IP3-рецептор, выделенный из мозжечка, может быть фосфорилирован cAMP-зависимой протеинкиназой , РКС и CaKMPK II (CaKM-зависимая протеинкиназа II) . Фосфорилирующая активность этих трех протеинкиназ аддитивна: каждая из них фосфорилирует IP3-рецептор, добавляя фосфатный остаток в своем собственном участке молекулы белка. Аминокислотная последовательность IP3-рецептора высоко консервативна, между белками мыши и крысы различие выявлено только в 21 аминокислотном остатке из 279. В IP3-рецепторе, два домена (с N-конца) обращены в сторону цитоплазмы. В наружнем домене молекулы расположен участок связывания IP3, в то время как примембранный домен является необходимым для контакта с мембраной и изменения конформации рецептора, которое вызывается связыванием IP3, и приводит к открыванию канала. СООН-концевой участок молекулы, который ориентирован в цитозоль, также включен в контроль открывания канала. СООН-концевая последовательность включает цистеин, через который может быть опосредован стимулирующий эффект таких соединений, как окисленный глютатион и тимеросал. Идентифицированы два участка, богатых глицином, которые, как предполагается, являются регуляторными местами связывания АТР. Четыре состояния проводимости канала можно объяснить, по-видимому, тетрамерной структурой белкового комплекса IP3-рецептора. Полагают, что тетрамерной структуре IP3-рецептора соответствует четыре Са2+-канала с проводимостью 20 пСм каждый в составе одного белкового комплекса.