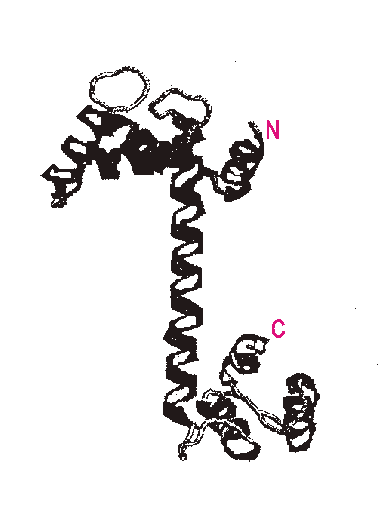Белки теплового шока (HSP, БТШ): введение
Все живые клетки отвечают на повышение температуры и некоторые другие стрессовые воздействия синтезом специфического набора белков, называемых белками теплового шока (БТШ, Hsp, heat shock protein, stress protein). У ряда бактерий обнаружена универсальная адаптивная реакция в ответ на различные стрессовые воздействия (высокие и низкие температуры, резкий сдвиг рН и др.), проявляющаяся в интенсивном синтезе небольшой группы сходных белков. Такие белки получили название белков теплового шока, а само явление - синдром теплового шока. Стрессовое воздействие на бактериальную клетку вызывает ингибирование синтеза обычных белков, но индуцирует синтез небольшой группы белков, функция которых предположительно заключается в противодействии стрессовому воздействию путем защиты важнейших клеточных структур, в первую очередь нуклеоидов и мембран. Еще не ясны те регуляторные механизмы, которые запускаются в клетке при воздействиях, вызывающих синдром теплового шока, но очевидно, что это универсальный механизм неспецифических адаптивных модификаций.
Как уже было сказано, к БТШ относят белки, синтезируемые клетками в ответ на тепловой шок, когда подавлена экспрессия основного пула белков, участвующих в нормальном метаболизме. Семейство 70 кДа БТШ ( БТШ-70 эукариот и DnaK прокариот) объединяет белки теплового шока, играющие существенную роль как в обеспечении выживания клетки в стрессовых условиях, так и в нормальном метаболизме. Уровень гомологии между белками прокариот и эукариот превышает 50% при полной идентичности отдельных доменов. 70 кДа БТШ являются одной из самых консервативных групп белков в природе ( Lindquist Craig, 1988 ; Yura et al., 1993 ), что связано, вероятно, с шаперонными функциями , которые эти БТШ выполняют в клетках
Индукция генов белков теплового шока (HSP) у эукариот происходит под воздействием фактора теплового шока HSF. В клетках, не подвергшихся стрессу, HSF присутствует и в цитоплазме и в ядре в виде мономерной формы, связанной с Hsp70 , и не имеет ДНК-связывающей активности. В ответ на тепловой шок или другой стресс, Hsp70 отсоединяется от HSF и начинает укладывать денатурированные белки. HSF собирается в тримеры, у него появляется ДНК связывающая активность, он аккумулируется в ядре и связывается с промотором. При этом транскрипция шаперонов в клетке возрастает во много раз. После того, как стресс прошел, освободившийся Hsp70 опять присоединяется к HSF, который при этом теряет ДНК-связывающую активность и все возвращается в нормальное состояние [ Morimoto ea 1993 ].Белки теплового шока появляются на поверхности клеток синовиальной оболочки при бактериальных инфекциях.
Большинство этих белков теплового шока образуются в ответ и на другие повреждающие воздействия. Возможно именно они помогают клетке пережить стрессовые ситуации. Существует три основных семейства белков теплового шока - семейства белков с мол. массой 25, 70 и 90 кДа ( hsp25 , hsp70 и hsp90 . В нормальных клетках было обнаружено множество очень похожих между собой белков из каждого из этих семейств. Они помогают переводить в раствор и вновь сворачивать денатурированные или неправильно свернутые белки. Есть у них и другие функции.
Лучше всего изучены белки семейства hsp70 . Эти белки связываются с некоторыми другими белками, а также аномальными белковыми комплексами и агрегатами, от которых потом освобождаются, присоединяя AТР. Они помогают переводить в раствор и заново сворачивать агрегированные или неправильно свернутые белки путем нескольких циклов присоединения и гидролиза AТР. Аномальные белки имеются в любой клетке, но при некоторых воздействиях, например при тепловом шоке, их количество в клетке резко возрастает, и, соответственно, возникает необходимость в большом количестве белков теплового шока. Что обеспечивается активацией транскрипции определенных генов теплового шока .
Белки теплового шока, образуя комплекс с растущей полипептидной цепью, предотвращают ее неспецифическую агрегацию и деградацию от действия внутриклеточных протеиназ, способствуя правильному фолдингу блков, происходящему с участием других шаперонов. Hsp70 принимает участие в ATP-зависимом разворачивании полипептидных цепей, делая неполярные участки полипептидных цепей доступными действию протеолитических ферментов.
Белки теплового шока кодируются семейством эволюционно устойчивых генов, которые экспрессируются в ответ на разнообразные стрессовые воздействия и участвуют в механизмах адаптации. Впервые открытые при термическом шоке у дрозофиллы, стресс-белки участвуют в большинстве физиологических процессов всех живых организмов и являются компонентом единого сигнального механизма [ Ananthan J., Goldberg A.L. 1986 , Massa S.M., Swanson R.A. 1996 , Morimoto R., Tissieres A. 1994 , Ritossa F. 1962 ].
Активация транскрипционных факторов стресс-белков (HSF) происходит путем их фосфорилирования под влиянием увеличения внутриклеточной концентрации кальция, свободнорадикальных реакций перекисного окисления липидов и других процессов оксидантного стресса , активации протеазных ингибиторов и тирозинкиназ. Но основным триггером , запускающим синтез стресс-белков, является дефицит ATP , сопровождающий недостаточное поступление в ткань мозга кислорода и глюкозы [ Benjamin I. J., Hone S. 1992 , Bruce J.L., Price B.D. 1993 , Cajone F., Salina M. 1989 , Courgeon A.-M., Rollet E. 1988 , Freeman M.L., Borrelli M.J. 1995 , Kil H.Y., Zhang J. 1996 , Suga S., Novak T.S., Jr. 1998 , Price B.D., Calderwood S.K. 1991 , Zhou M., Wu X. 1996 ].
Существуют несколько классов транскрипционных факторов стресс- белков, среди которых белок HSF1 является медиатором ответа на стресс, a белок HSF2 - регулятором hsp-генов . В условиях церебральной ишемии HSF1 и HSF2 синергично активируют генную транскрипцию. Они образуют активированные тримеры, которые связываются с регуляторными последовательностями (HSE) в промоторных зонах стресс-генов, что приводит к синтезу мРНК. Накопление стресс-белков ведет к "включению" ауторегуляторной петли, прерывающей их дальнейшую экспрессию [ Baler R., Zou J. 1996 , Mestril R., Ch, S.-H. 1994 , Sistonen L, Sarge K.D. 1994 , Rabindran S.K., Haroun R.I. 1993 , Sarge K.D., Murphy S. 1993 , Sorger P.K., Pelham H.R.B. 1987 , Wu C., Wilson S. 1987 , Nakai A., Morimoto R. 1993 , Nowak T.S., Jacewicz M. 1994 , Scharf K.-D., Rose S. 1990 , Schuetz T.J., Gallo G.J. 1991 ].
В экспериментальных моделях с фокальной ишемией мозга установлено, что экспрессия гена основного стресс-белка - белка HSP72 - регистрируется в ограниченной области мозга с уровнем снижения мозгового кровотока ниже 50% от нормы и только в клетках, остающихся жизнеспособными. Соответственно в ядерной зоне ишемии экспрессия гена hsp72 отмечается преимущественно в клетках эндотелия сосудов, более резистентных к ишемии; в маргинальной области инфаркта - и в глиальных клетках, в зоне пенумбры - и в нейронах [ Nowak T.S., Jacewicz M. 1994 , Nowak T.S., Zhou Q. 1999 , Gonzalez M. F., Shiraishi K. 1989 , Kinouchi H., Sharp P. 1993 ].
Экспрессия генов других стресс-белков различна в разных клеточных пулах. Так, экспрессия гена hsp27 преимущественно зарегистрирована в астроцитах , гемоксигеназы-1 (НО-1 , ген hsp32) - в микроглиальных клетках [ Kato H., Kogure K. 1994 , Kato H., Kogure K. 1995 ].
Проведенные исследования позволили предположить нейропротективную роль стресс-белков. Показано, что HSP72-позитивные клетки в зоне пенумбры легче всего переживают острую ишемию [ States B.A., Honkaniemi J. 1996 ].
См. также ТРАНСКРИПЦИОННЫЕ ФАКТОРЫ: КЛАСС: ТФ 3.4 факторы теплового шока
Ссылки:
- Фолдинг и системы защиты вновь синтезированных полипептидных цепей от деградации
- Hsp70: общие сведения
- ИЗСД: сравнение концепций аутоиммунного разрушения B-клеток
- Протоонкогены: превращение в онкогены (активация)
- Митохондрии: цитоплазматические факторы, влияющие на импорт белков
- Полифункциональность полипептидов
- Ревматоидный артрит: общие сведения (0477)
- Hsp (Белки теплового шока, БТШ) дрожжей
- Полиаденилирование: влияние на время полужизни бактериальных мРНК
- Лимфома: сокращения
- Промоторы генов адаптивных белков
- Шапероны и стресс
- Микоплазмы: оперон генов БТШ
- BiP/GRP78 Белки
- Рецепторы глюкокортикоидов: Связывание гормона