Саркомер
Функциональной единицей мышечного волокна является миофибрилла . Миофибриллы занимают практически всю цитоплазму мышечного волокна, оттесняя ядра на периферию. Каждая миофибрилла имеет периодическое строение: толстые и тонкие филаменты образуют периодический рисунок вдоль каждой миофибриллы ( рис. 30.4 ; рис. 30.5 ). Регулярно повторяющийся элемент этого рисунка называется саркомером (от греч. sarco - мышца, mere - маленький).
Саркомеры соседних миофибрилл расположены друг против друга, отчего все мышечное волокно тоже приобретает периодическое строение.
Саркомер имеет длину около 2.5 мкм. Граница между двумя саркомерами имеет вид темной полосы на электронно-микроскопических фотографиях и носит название Z-диска . В Z-диске локализуется актин-связывающий белок альфа-актинин , который необходим для прикрепления актиновых филаментов к Z-диску. Колокализуются с альфа-актинином винкулин и интегрин ( Volk T. et al., 1990 ) ( рис.1-32 )
От Z-диска перпендикулярно ему отходят нити F-актина , ассоциированные с тропомиозином и тропонином . Актиновые филаменты , на зываемые также в данном случае тонкими нитями , имеют одинаковую длину около 1 мкм, таким образом, что тонкие нити, идущие от противоположных Z-дисков навстречу друг другу, не перекрываются. С тонкими нитями в скелетных мышцах ассоциирован гигантский белок небулин с молекулярной массой 500-800 кД ( Locker R.H., Wild D.J., 1986 ).
В центральной части саркомера вдоль его оси расположены миозиновые биполярные филаменты , длиной около 1.6 мкм и толщиной около 15 нм. Они называются также толстыми филаментами . На поперечном срезе видно, что миозиновые филаменты располагаются на равном расстоянии друг от друга, образуя гексагональную решетку. Концы тонких и толстых филаментов перекрываются. При этом тонкие филаменты находятся в промежутках между толстыми, равномерно окружая их.
Кроме миозина природные толстые филаменты содержат или ассоциированы с C-белком , H-белком ( белок 86 кД ), M-белком , миомезином , MM-креатинкиназой , титином , АМФ-дезаминазой , скелемином . С-белок с молекулярной массой 140 кД имеется в наибольшем количестве. Функция его неизвестна. По структуре он сходен с белками межклеточной адгезии серии N-CAM . Титин или коннектин образует очень тонкие эластичные филаменты, связывающие миозиновые филаменты c Z-пластинкой и ответственные за расположение миозиновых филаментов в центре саркомера. Титин - это самый большой из описанных к настоящему времени белков. Его молекулярная масса составляет порядка 2800 кД ( Maruyama K., 1986 ).
См. " Скелетные мышцы: структура ".
Ссылки:
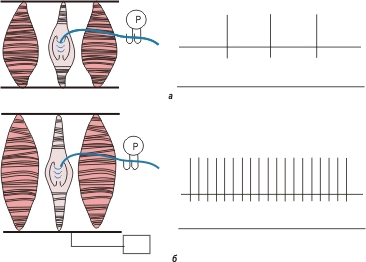
- Соотношение между частотой и напряжением мышечного волокна
- Электромеханическое сопряжение волокон скелетных мышц
- Физиологические и патологические сигналы мышечного реконструирования
- Гладкие мышцы: структура
- Соотношение между длиной мышцы и ее напряжением
- Механика сокращения одиночного мышечного волокна: общие сведения
- Митохондрии: организация в скелетных мышцах
- Модель скользящих нитей: общие сведения
- Мышечное волокно: общие сведения
- Молекулярные механизмы сокращения скелетной мышцы: общие выводы
- Болезнь центрального стержня
- T-Трубочки мышечных волокон (поперечные трубочки) скелетных мышц
- Механика сокращения одиночного мышечного волокна: резюме
- Мышцы: сокращение, роль ионов кальция
- КАРДИОМИОПАТИЯ СЕМЕЙНАЯ ГИПЕРТРОФИЧЕСКАЯ (CMH, FHC): ГЕНЕТИКА